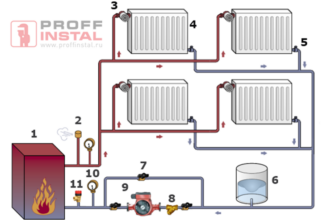
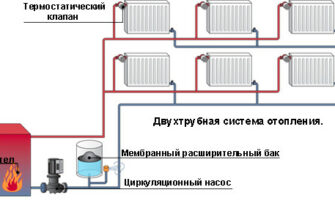
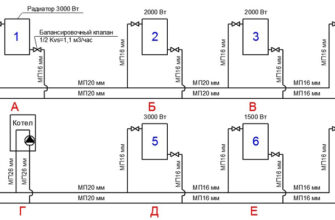
Влияние водорода на алюминиевые радиаторы
Какой бы алюминий не был: первичный, вторичный, экструзионный или литой — у него есть один очень важный недостаток. Не всегда этот факт останавливает покупателей при выборе данного оборудования, и со временем появляются проблемы.
При контакте теплоносителя с алюминиевой поверхностью алюминий сам себя защищает, образуя оксидную пленку Al2O3 — соединение алюминия и кислорода. Важный момент заключается в том, что защитный слой не пускает теплоноситель дальше, в отличие от коррозии металла. Казалось бы, что этот факт надо отнести к плюсу алюминиевых радиаторов, но есть одно большое «но».
Водород
Существует такое значение, как водородный показатель, который обозначается латинскими буквами «pH». Алюминий чувствует себя хорошо при показателе в 7-8 pH. К семи pH можно отнести чистую воду, а к восьми pH — морскую. Но не исключено содержание в чистой воде большого количества сероводорода.
Если говорить простым языком, то цифра 7 — это нейтральная среда. Все, что выше этой цифры — щелочь, все, что ниже — кислота.
Алюминиевый радиатор комфортно себя чувствует в нейтральной среде. При показателях выше, чем 7 pH или ниже этого показателя, алюминиевая защитная пленка начинает размываться, а алюминий будет пытаться восстановить защитный слой, выделяя при этом водород. Этот процесс и является губительным фактором для алюминиевого радиатора. В большинстве случаев губительный эффект происходит в неотопительный сезон.
Почему?
Технический паспорт радиатора не всегда расскажет, что после отопительного сезона необходимо перекрывать запорную арматуру на радиаторах во избежание многих критических факторов. Это лишь предосторожность. Еще считается необходимым при закрытой арматуре открывать краны Маевского на время летнего периода.
В застоявшейся воде в радиаторах образуются бактерии, которые меняют состав воды. Химдобавки, которые присутствуют в воде благодаря очистным станциям, тоже меняют воду. В такой воде показатель pH меняется в ту или иную сторону, и образовавшийся водород должен выйти. При закрытых кранах Маевского даже самая стойкая секция радиатора не выдерживает и дает трещину. На протяжении всего неотопительного сезона давление в закрытых емкостях растет каждый день.
В многоэтажном доме с центральным отоплением алюминиевые радиаторы устанавливать не рекомендуется. Что касается частных домов, то всегда можно обеспечить для радиаторов оптимальную среду в 7 pH.
Не рекомендуется устанавливать теплообменник, если в системе отопления присутствует медная часть или магистраль из медных труб. Обычно такие теплообменники установлены в двухконтурных котлах, а также все обвязочные трубы у настенных котлов выполнены из меди. Как и в электронике, медь и алюминий несовместимы. И, несмотря на то, что алюминий вырабатывает защитный слой, реакции все же присутствуют.
Преимущества алюминиевого радиатора
Что можно отнести к плюсу алюминиевого секционного радиатора? Проходной канал между проточным верхним и нижним коллектором больше, чем у биметаллического радиатора. Это способствует лучшему протоку теплоносителя, обеспечивая более быстрый обогрев всей площади радиатора.
Алюминиевый радиатор немного дешевле биметаллического, а по тепловой мощности без специальных приборов разницы не почувствовать. Рекомендуется устанавливать только в частных домах, коттеджах и на даче. Преимущество секционного радиатора заключается в добавлении секций до нужной длины путем соединения, в отличие от стальных радиаторов, где неправильный расчет перед установкой или необходимость увеличения мощности радиатора влечет за собой полную замену оборудования.
Материал подготовлен при поддержки интернет-магазина Теплоторг.
Алюминиевые радиаторы. Мифы и реальность
Алюминиевые радиаторы, что может быть лучше? Вес в 2,5-3 раза меньше, чем у железа или чугуна, а теплопроводность в 3 раза больше чем у железа и в почти 5 раз больше, чем у чугуна.
Что даёт вес, всем понятно, это меньше нагрузка на крепления, на стену, меньше вес при транспортировке и подъёме на этаж. Теплопроводность, это способность материала проводить через себя тепло, чем она выше, тем быстрее металл радиатора отдаёт энергию теплоносителя и тем быстрее охлаждается, когда нагрев не нужен.
Алюминий — идеальный материал для радиаторов. Лёгкий и красивый. Круче него только медь, которая по теплопроводности уделывает алюминий, но тяжелее железа и более дорогая.
Но так ли идеален алюминий? Рассмотрим его свойства и разные нюансы.
Алюминий при реакции с воздухом (кислородом), образует на своей плоскости тонкую плёнку из оксида алюминия, которая не реагирует далее с водой и кислотами, но достаточно легко растворяется щелочами.
4Al+3O2 = 2Al2O3 Или с водой, образуя ту же самую оксидную плёнку и свободный водород. 2Al+3H2O = Al2O3 +3H2
Всем известна эта проблема с выделяемым водородом на алюминиевых радиаторах. Но она не так долга, всё закончится когда на поверхности алюминия образуется эта защитная плёнка оксида. Когда в описании к алюминиевым радиаторам вы читаете, что на внутренней поверхности есть защитное покрытие, значит, скорее всего, производитель уже дал поверхности покрыться оксидом, поместив секции радиатора в воду или же во влажный воздух. Если плёнки оксида ещё нет, она появится при контакте с теплоносителем (если это вода), при этом какое-то время выделяемый водород будет удаляться автоматическими воздухоотводчиками, снижая давление в системе, при этом некоторые паникуют, думая, что у них есть утечка.
Иногда при разных нюансах, оксидная плёнка может повреждаться мусором, песком в системе отопления, после чего идёт новая реакция алюминия с водой и нарастания плёнки оксида. Это весьма скоротечный процесс, потому как повреждения плёнки обычно минимальны.
На этом все злоключения пользователя с алюминиевыми радиаторами заканчиваются, если у него автономная система и вода в качестве теплоносителя. Если какая-то «незамерзайка», то тут могут быть нюансы. Стандартные «незамерзайки» на основе пропиленгликоля (которые рекомендованы для систем отопления в силу их меньшей агрессивности, чем этиленгликолевые), никак не реагируют с алюминием. Но самодельные «бадяжные» смеси могут нарушать целостность оксидной плёнкт на алюминии.
Если вдруг так случилось, что пользователь рискнул поставить алюминиевый радиатор на центральное отопление, то это равносильно бомбе замедленного действия. Что же происходит при этом?
Не секрет, что в системах центрального отопления, в теплоноситель добавляется щёлочь для промывки всех её частей (особенно металлических), препятствованию коррозии. При этом постоянно поддерживается щелочной pH.
При этом идёт реакция защитной плёнки из оксида алюминия и растворённой щёлочи в теплоносителе.
Al2O3+2NaOH + 7H2O = 2Na[Al(OH)4(H2O)2] который позже распадается на 2NaAlO2+8H2O то есть на алюминат натрия и воду. Но и это соединение не стабильно и снова реагирует с водой, становясь тетрагидроксоалюминатом натрия Na[Al(OH)4]. Но и эта комплексная соль нестабильна и распадается на другие комплексные соли, но это не главное, главное, что плёнка оксида алюминия перстаёт защищать алюминий основания. и он начинает реагировать со щёлочью теплоносителя
2Al+2NaOH+6H2O = 2Na[Al(OH)4]+3H2 Снова с выделением водорода и образованием тетрагидроксоалюмината натрия. Так щёлочь теплоносителя съедает тело радиатора. Продукты же реакции уносятся теплоносителем и доставляется новая порция щелочного теплоносителя. Алюминий просто вымывается щёлочью.
Со временем в каких-то утончившихся местах радиатор может лопнуть от того, что слой алюминия не выдерживает давления в системе отопления (либо при гидроударе).
Но тут ещё накладываются нюансы изготовления алюминевых радиаторов. Рассмотрим и их.
Если радиаторы сделаны путём литья, когда алюминий расплавлен, а потом влит в формы и он создал кристаллическую структуру, то его структура примерно такова
Где серые шарики — атомы алюминия. Пока щёлочь теплоносителя не съест первый ряд атомов, она не приступит к к следующему ряду (так как атомы идентичны, раствор щёлочи равномерен в концентрации и время взаимодействия одинаково). Так будет, если радиатор получен путём литья.
Но ведь есть более продвинутая и дешёвая технология — порошковое прессование. В ней разделяют 4 главных процесса:
1. Приготовление порошка.
2. Смешивание.
3. Прессование.
4. Спекание.
Итак, если у вас нормальный производитель, он выдержит всю технологию и вы получите качественное, но дорогое изделие. А так как сейчас идёт борьба за удешевление (а значит борьба за покупателя или за прибыль), то некоторые нерадивые производители из стран отдалённых (ну вы понимаете), могут вносить в технологию следующие погрешности.
1. Приготовление порошка может идти с нарушением его фракции, то есть укрупнения частиц. Так как именно порошок в порошковой металлургии самый застратный момент, его стараются удешевить. При этом может появляться порошок с гранулами вот такого размера
2. Смешивание. Чтобы ещё более удешевить порошковую смесь алюминия, её могут смешать с другими, более дешёвыми порошками, например силумином, цинком, железом, чугуном, а при пущей наглости пластиком или даже мусором. Можно также нетщательно еремешать порошки между собой.
3. Прессование. При прессовании происходит так, что гранулы порошка прижимаются друг к другу некоторыми частями с такой силой, что происходит «зацеп» кристаллической решётки на атомарном уровне. Так между гранулами образуется пятно котнтакта, где материалы как бы склеиваются между собой. Обычно необходимо при этом обрабатывать пресс-формы ультразвуком для большей усадки и большей плотности проникновения между гранулами, но это ведь лишние траты для того производителя, который решил сэкономить.
4. Спекание. Это процесс, когда полученную деталь нагревают ниже температуры плавления материала, но при этом пятно контакта между гранулами увеличивается и деталь становится гораздо крепче. Тут тоже можно сэкономить, уменьшив время спекания или температуру.
И что тогда в этом случае мы получаем в разрезе. Возьмём тот же самый рисунок как с литьём, но теперь наши атомы алюминия станут гарнулами порошка (естественно гранулы несравнимо больше чем атомы)
Теплоноситель получит гораздо большую площадь реакции, при этом увеличится её скорость, то есть съедать алюминий щелочной теплоноситель будет быстрее. Заодно так выкусывая из тела радиатора целые гранулы неалюминия, он будет гораздо быстрее утоньшать стенку радиатора, что приведёт к более быстрой поломке.
Теперь рассмотрим распространённый миф, что если алюминиевый радиатор с щелочным теплоносителем закрыть герметично в радиаторе (перекрыть краны подачи и обратки), со временем от выделенного из-за реакции алюминия со щёлочью водорода, радиатор может взрваться-лопнуть.
Во-первых, при такой реакции всегда есть растворённый водород, который не существует в виде свободного газа. Он не будет существовать до тех пор, пока давление в пузыре водорода, который выделился в свободном виде, будет выше давления в теплоносителе. Чтобы было понятнее, вспомните бутылку газированной воды. Пока она закрыта, есть небольшая полость у горлышка бутылки, где есть газ, но из воды он не выделяется, так как давление воды равно давленю в этой полости с газом. Но стоит только открыть бутылку и снизить давление, растворённый в воде газ быстро себя проявляет. Но стоит снова закрыть бутылку, через время пузырьки газа вновь перестают выделяться, пока давление не выровняется.
Так же и в радиаторе, газ сначала будет растворяться в теплоносителе, потом освободит себе какую-то полость в верхней части радиатора, откуда выместит теплоноситель, за счёт чего повысится несколько давление в теплоносителе. Но газ очень сжимаем, а жидкость нет, поэтому накачать эту газовую полость водородом до такой степени, чтобы она вытеснила много воды и создала критическое давление, это нужно очень много водорода.
А почему же мы не сможем получить так много водорода? Потому как количество щёлочи в нашем запертом радиаторе неизменно и с каждой прореагировавшей молекулой алюминия, концетрация щёлочи становится всё меньше, ведь она разлагается на описанные выше комплексные соли.
Почему же иногда закрытые радиаторы таки взрываются? Именно по описанной выше причине — некачественное порошковое прессование, которое приводит к тому, что катастрофически утоньшается стенка в каком-то месте из-за примесей и отхода от технологии, и радиатор не выдерживает внутреннего давления, а не из-за критического давления ввиду выделения водорода.
Но при всех причинах, которые обслуживающая отопление контора может рассказать пользователю по поводу взорвавшегося радиатора, вина лежит только на пользователе. Ибо нельзя ставить алюминиевые радиаторы для эксплуатации с щелочным теплоносителем. Для этого давно уже придуман биметалл.
Химические процессы в алюминиевых радиаторах
Хорошо известны сомнения проектировщиков и монтажников относительно приемлемости установки алюминиевых радиаторов в той или иной отопитель-ной системе. В одних случаях они беспроблемно работают долгие годы, в других — постоянно заполняются каким-то газом, корродируют и в результате довольно быстро разрушаются. Из-за чего это происходит? О причинах химических процессов, происходящих в отопительных приборах из алюминия, мы и поговорим в данной статье.
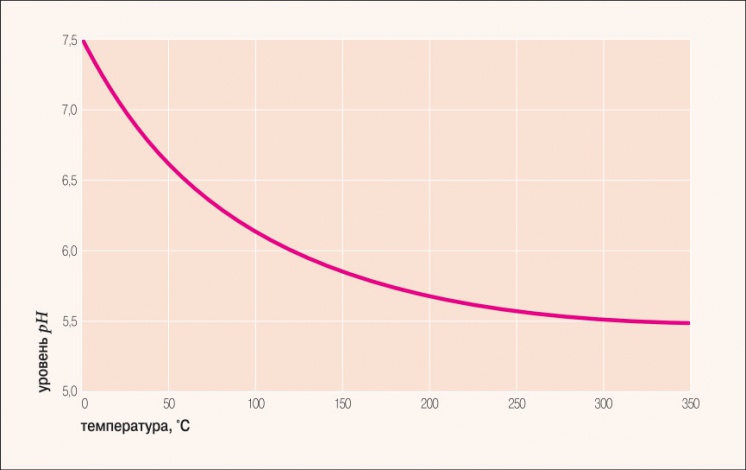
Рис. 1. Водородный показатель дистиллированной воды в зависимости от температуры
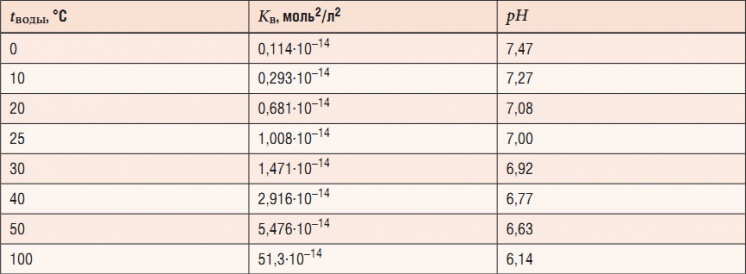
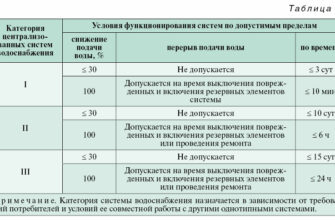
Табл. 1. Значения нейтрального pH в чистой воде при различных температура
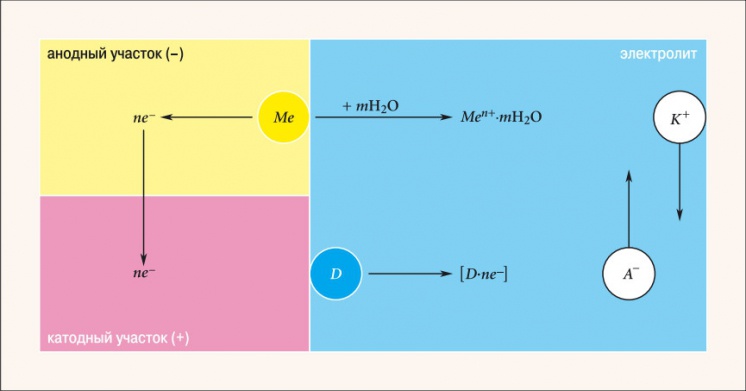
Рис. 2. Схема электрохимического коррозионного процесса
Табл. 2. Значения электродных потенциалов некоторых элементов
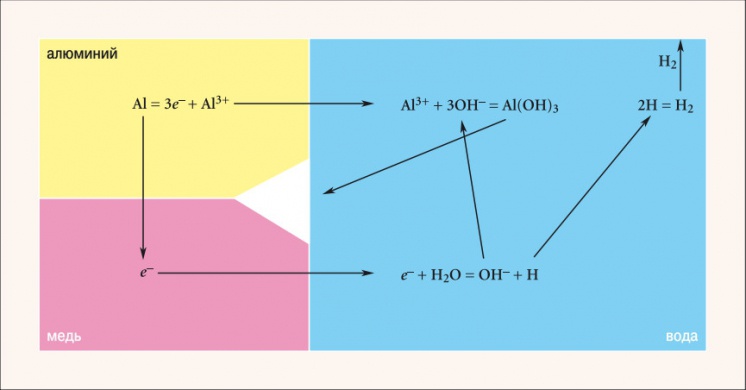
Рис. 3. Схема процесса коррозии при контакте алюминия и меди
Алюминиевые радиаторы очень удобны: они компактны, эстетичны, обладают малой инерционностью и очень высокой теплоотдачей. Теплопроводность изделий из алюминиевых сплавов — 202–236 Вт/(м⋅K). Из металлов, используемых для изготовления радиаторов, выше эта величина только у меди: 382–390 Вт/(м⋅K). У других материалов теплопроводность ниже в разы. При этом алюминий как сырье примерно в два раза дешевле меди.
В то же время с алюминиевыми радиаторами связано множество предрассудков, основанных на незнании потребителем природы химических процессов, происходящих внутри отопительной системы, — существует, например, устойчивое мнение, что с алюминиевыми радиаторами нельзя использовать медные и оцинкованные трубы. Но почему и какому из материалов от этого будет хуже — знают не все. Известно также, что алюминий предъявляет высокие требования к pH теплоносителя. Насколько это серьезно и чем грозит превышение? Попробуем разобраться.
Если не брать в расчет ошибки при расчетах максимального давления, гидроудары и производственный брак, самой распространенной проблемой в алюминиевых радиаторах является т.н. «завоздушивание», в результате которого повышается нагрузка на воздухоотводчик, увеличивается объем подпитки, при неблагоприятном раскладе может лопнуть секция.
На самом деле, выделяющийся газ — это водород H2, продукт взаимодействия алюминия с разнообразными веществами. Происходит данный процесс в трех случаях: реакция алюминия с теплоносителем-водой, реакция алюминия с теплоносителем-гликолем, электрохимическая коррозия алюминия.
Водородный показатель
В первую очередь, возникает вопрос, каким образом алюминий вообще может вступать в реакцию с чем бы то ни было: ведь на воздухе (т.е. сразу после изготовления на заводе) на его поверхности образуется тонкая прочная беспористая оксидная пленка Аl2О3, защищающая металл от дальнейшего окисления и обусловливающая его высокую коррозионную стойкость.
Кроме того, производители дополнительно покрывают внутренние поверхности радиаторов различными составами, препятствующими доступу теплоносителя к алюминию. Поэтому, чтобы «добраться» до металла, надо сперва разрушить оксид.
Самый простой способ — механическое воздействие твердых частиц, которые могут присутствовать в теплоносителе: они вызывают абразивный износ и разрушают защитный слой на внутренней поверхности прибора. Данная проблема легко решается установкой фильтров и грязевиков в нужных местах отопительной системы.
Более интересную ситуацию представляет собой «химическая атака». Она связана с амфотерностью оксида алюминия, т.е. его способностью проявлять как кислотные, так и основные свойства: взаимодействовать как с щелочами, так и с кислотами с образованием солей, хорошо растворимых в воде (это значит, что они не остаются на металле, а поступают в теплоноситель). Пример реакции с кислотой (свойства основного оксида):
Пример реакции с водным раствором щелочи (свойства кислотного оксида):
Взаимодействует оксид алюминия, правда, не со всеми соединениями: так, серная или азотная кислоты разрушения пленки не вызовут.
Важнейшим индикатором наличия в воде растворенных кислот является водородный показатель pH (по первым буквам латинских слов potentia hydrogeni — сила водорода или pondus hydrogenii — вес водорода) — концентрация ионов водорода H + в растворе, количественно выражающая его кислотность, вычисляется как отрицательный (взятый с обратным знаком) десятичный логарифм активности водородных ионов в молях на литр:
Вообще, в химии сочетанием pX принято обозначать величину, равную –lgX, а буква H в данном случае обозначает концентрацию ионов водорода H + . Несколько меньшее распространение получила обратная pH величина — показатель основности раствора pOH, равный отрицательному десятичному логарифму концентрации в растворе ионов OH – : pOH = –lg[OH – ].
В чистой воде при 25 °C величины концентрации ионов водорода H + и гидроксидионов OH – одинаковы и составляют 10 –7 моль/л. Это напрямую следует из определения ионного произведения воды, гласящего, что произведение концентраций ионов водорода Н + и ионов гидроксида OH – в воде или в водных растворах при определенной температуре равно константе Kв. Нормальными условиями принято считать 25 °C, при которых Kв = 10 –14 моль 2 /л 2 . Таким образом, при 25 °C — pH + pOH = 14.
Когда концентрации обоих видов ионов в растворе одинаковы, говорят, что раствор имеет нейтральную реакцию. При добавлении к воде кислоты концентрация ионов водорода увеличивается, а концентрация гидроксидионов, соответственно, уменьшается. При добавлении основания, наоборот, повышается содержание гидроксидионов, а концентрация ионов водорода падает. При [H + ] > [OH – ] раствор называют кислым, при [OH – ] > [H + ] — щелочным.
Для удобства представления, чтобы избавиться от отрицательного показателя степени, вместо концентраций ионов водорода пользуются их десятичным логарифмом, взятым с обратным знаком, который и назвали водородным показателем pH.
При более высоких температурах константа диссоциации воды повышается, соответственно увеличивается ионное произведение воды, поэтому нейтральной оказывается pH + , так и OH – ); при понижении температуры, напротив, нейтральный pH возрастает. В табл. 1 и на рис. 1 показаны изменения значения нейтрального pH в чистой воде в зависимости от температуры.
При сильных отклонениях значения pH от нейтрального можно с достаточной степенью уверенности говорить о наличии в воде растворенных кислот или оснований, которые могут вступать в реакцию с оксидом алюминия или с защитным покрытием, нанесенным производителем, разрушая их и обнажая алюминий. Из этого следует также, что применять химические реагенты для контроля жесткости теплоносителя в случае с алюминиевыми радиаторами надо с большой осторожностью. В идеале вода должна быть дистиллированной.
Реакция алюминия с теплоносителем
Если оксид алюминия Al2O3 с классическими окислителями в реакцию не вступает, сам алюминий после контакта с водой преобразуется в гидроксид (тоже, к слову, амфотерное соединение) с выделением водорода:
Если же pH теплоносителя далек он нейтрального, этот же газ будет выделяться в качестве продукта реакции алюминия с щелочами и некоторыми кислотами с образованием растворимых солей:
Если в качестве теплоносителя используется незамерзающая жидкость, то ситуация будет сходная. При взаимодействии водного раствора этиленгликоля, самого распространенного антифриза, с алюминием происходит замещение гидроксильного водорода на металл и выделение свободного водорода Н2.
Электрохимическая коррозия
Электрохимическая коррозия — наиболее распространенный вид коррозии металлов. При контакте двух металлов, обладающих разными электродными (электрохимическими) потенциалами и находящихся в электролите, образуется гальванический элемент (рис. 2). Поведение металлов зависит от значения их электродного потенциала. Металл Me, имеющий более отрицательный электродный потенциал (анод), переходит в качестве положительно заряженных ионов Men + в раствор. Избыточные электроны ne – перетекают по внешней цепи в металл, имеющий более высокий электродный потенциал (катод). Катод при этом не разрушается, а электроны из него ассимилируются какими-либо ионами или молекулами раствора (деполяризаторами D), способными к восстановлению на катодных участках. Чем ниже электродный потенциал металла по отношению к стандартному водородному потенциалу, принятому за нулевой уровень, тем легче металл отдает ионы в раствор, тем ниже его коррозионная стойкость. Значения электродного потенциала Е0 некоторых элементов приведены в табл. 2. Расположение металла выше (хотя обычно говорят «левее») водорода означает, что он способен вытеснить водород из соединений (воды, кислот и пр.).
Теперь рассмотрим конкретный пример: пару «медь–алюминий». Сразу отметим, что для возникновения разности потенциалов требуется непосредственный контакт двух металлов (алюминиевый радиатор и медный фитинг), а не просто наличие их в системе (алюминиевый радиатор, медный теплообменник, металлопластиковые трубы). Во втором случае имеет место разрыв цепи, поэтому электроны никуда перетекать не смогут. Использование диэлектрических вставок — самый надежный способ предотвращения неконтролируемой миграции заряженных частиц.
И еще одно замечание, касающееся направления движения электролита: реакция пойдет лишь в случае, если анод расположен «ниже по течению» относительно катода (медный фитинг на входе в алюминиевый радиатор). Правда, если будут моменты простоя системы без движения теплоносителя, это замечание значения не имеет.
Алюминий обладает большей способностью отдавать электроны по сравнению с медью, что видно из значений их стандартных электродных потенциалов (–1,66 и +0,34 соответственно). Следовательно, в случае замкнутой цепи медь является катодом, а алюминий — анодом (рис. 3). Ионы алюминия Al 3+ из кристаллической решетки переходят в раствор, образуя вместе с гидроксидионами OH – гидроксид алюминия Al(OH)3, а электроны поступают в медь. Оторванные от воды потерявшие электрон ионы водорода H + используют их для объединения в молекулу H2. Коррозия алюминия продолжается, т.к. электроны непрерывно уходят из него, смещая тем самым равновесие в сторону образования ионов. Ход электрохимического процесса определяется разностью потенциалов элемента. Для пары «медь–алюминий» разность потенциалов составляет 2 В. Если взять пару «цинк–алюминий», то разность будет менее значительной — 0,9 В, а, значит, реакция пойдет в два раза медленнее.
Подведем итоги
Если при проектировании и монтаже будут приняты меры по предотвращению описанных выше процессов, алюминиевые радиаторы отлично прослужат десятки лет. Изолирующие диэлектрические вставки и контроль состава теплоносителя позволят заказчику наслаждаться отопительным прибором с множеством положительных характеристик: высокая теплоотдача, пластичность (т.е. устойчивость к гидроударам), небольшой вес, возможность легко изменять мощность путем добавления или удаления секций и пр.